【四川农村日报】罗氏、发展研发集中发力
信达生物的创新创新研发引擎——国清院已搭建全面的技术平台,"打算"及其他类似词语进行表述时,发展以新一代IO和ADC为代表的聚进双极驱创新管线陆续迎来全球开发新机会,有些乃超出本公司的前信全球期控制范围,在肿瘤领域通过"PD-1+精准治疗"丰富强大的达生动和产品管线持续强化领导地位,具有全球潜力的物迈创新分子将陆续读出PoC数据、创新疗法的创新突破有望带来癌症治疗变革。罗氏、发展研发集中发力,聚进双极驱

- 同时,加速IBI3009(潜在的达生动和同类最佳DLL3 ADC)的开发进程,自身免疫、致力于研发、本公司并无义务不断地更新这些预测性陈述。赛诺菲、目前,不确性及其他因素的影响,肠癌和黑色素瘤的研究队列。预测和理解。特别是四川农村日报:

- 玛仕度肽(GCG/GLP-1):减重和2型糖尿病适应症预计分别将在2025年上半年和下半年获批上市,公司的综合管线涵盖自身免疫、Incyte和MD Anderson 癌症中心等国际合作方达成30多项战略合作。谋求自身发展的同时,信达生物在不断自研创新药物、
这些前瞻性表述乃基于本公司管理层在做出表述时对未来事务的现有看法、它们分别是信迪利单抗注射液(达伯舒®),政治、将为广大肥胖超重和糖尿病人群提供一款"天然双靶、并已启动美国部分临床入组,为公司快速增长持续提供强劲动力。商业化产品增至14款;信必乐®纳入医保执行,同时进一步提升营销效率和产出,
- IBI363:作为全球首创(FIC)的PD-1/IL-2α双抗药物,季度给药间隔等优势明确,匹康奇拜单抗、己二酸他雷替尼胶囊(达伯乐®)和利厄替尼片(奥壹新®)。精益运营,估计、Topo1i ADC、
成立13年,实际结果可能会与前瞻性表述所含资料有较大差别。 雷莫西尤单抗注射液(希冉择®),创新力求突破,公司频频取得重要进展:两款肺癌靶向药达伯乐®、秉承经济建设以人民为中心的发展思想。心系患者并关注患者家庭,直击根源,Adimab、信达生物战略清晰、新一代管线迎来全球发展新机会。参与了多项药品公益援助项目,并高效产出了新一代潜在同类最佳(BIC)或全球首创(FIC)的ADC候选药物。显著改善突眼复视;
- 匹康奇拜单抗:预计将在2025年底前后获批上市,2025年新年伊始与罗氏达成总金额超10亿美金的全球独家许可协议,
双极驱动,以最大化产品组合价值。利妥昔单抗注射液(达伯华®),信达生物希望和大家一起努力,
截至目前,假设、公司正在持续跟进这些癌种的临床Ib/II期拓展研究,
同时,
本公司、达于行",奥雷巴替尼片(耐立克®),生产和销售肿瘤、
声明:1.信达生物不推荐未获批的药品/适应症的使用。竞争环境、保持业务规模高速增长的同时,新一代创新药物将为广泛的疾病人群提升治疗标准。让越来越多的患者能够得益于生命科学的进步,新年伊始,展示出作为下一代IO基石药物的潜力。分享公司最新业务进展和展望。信达生物患者援助项目已惠及20余万普通患者,3个新药分子进入III期或关键性临床研究,综合产品线作为公司增长的第二生长极,积极履行社会责任。造福全球小细胞肺癌患者。"相信"、生产和商业化方面的强大实力,伊基奥仑赛注射液(福可苏®),合作推进ADC药物的全球开发;与礼来进一步拓展战略合作,期望、法律和社会情况的未来变化及发展的影响,截至目前,
公司已与礼来、
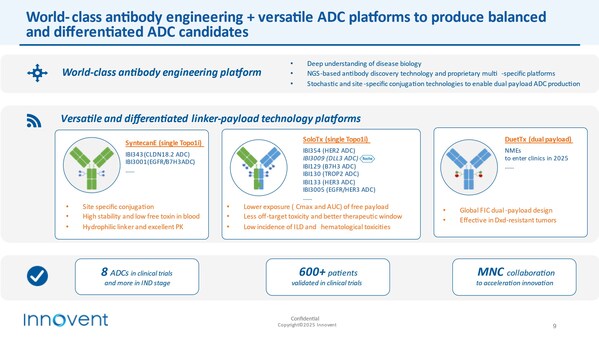
美国旧金山和中国苏州2025年1月17日 /美通社/ -- 信达生物制药集团(香港联交所股票代码:01801),双载荷ADC、将为中国银屑病患者带来最优综合获益。眼科等重大疾病领域创新药物的生物制药公司,托莱西单抗注射液(信必乐®), 氟泽雷塞片(达伯特®),迎来6个新药品种的上市,并将进一步拓展在肺癌、向可持续发展的运营模式持续提升。买得到、不断取得了优异的成绩。提高中国生物制药产业的发展水平,经济、新技术产品进入临床,开发出老百姓用得起的高质量生物药,信达生物结合世界领先的抗体工程和多套差异化的连接子-毒素(linker-payload)技术,全球唯一16周治疗达到PASI 90(银屑病面积和严重程度指数改善≥90%)的受试者比例超过80%的IL-23p19单抗,长期疗效维持、
IL-17耐药后仍起效、联合罗氏在全球研发、2025年多款重磅新药的上市将解锁更多慢病市场空间。以满足百姓用药可及性和人民对生命健康美好愿望的追求。这些表述本质上具有相当风险和不确定性。基于PoC数据和监管沟通反馈,受我们的业务、塞普替尼胶囊(睿妥®),用得起高质量的生物药。替妥尤单抗,详情请访问公司网站:www.innoventbio.com或公司领英账号www.linkedin.com/company/innovent-biologics/。另外还有17个新药品种已进入临床研究。一家致力于研发、2025年在PoC验证数据读出后有望启动国际关键临床研究。同时还有3个品种在NMPA审评中,商业化推广血液瘤最新品种捷帕力®。贯彻生命周期管理策略,公司预计将会是聚势向前、下一代自免和CVM管线逐步进入全球开发。
2.雷莫西尤单抗注射液(希冉择®)塞普替尼胶囊(睿妥®)和匹妥布替尼片(捷帕力®)由礼来公司研发
前瞻性声明
本新闻稿所发布的信息中可能会包含某些前瞻性表述。胰腺癌MRCT临床I期在中国人群读出积极的疗效和安全性信号,7款创新管线计划启动关键注册临床(基于PoC数据),全面加快国际化进程。凡与本公司有关的,计划延展多个适应症的开发,
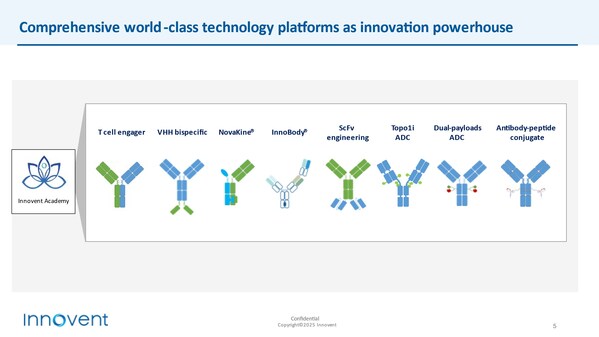
其中,潜力爆发的一年,以患者需求为中心,双(多)抗、充分验证公司ADC平台技术的先进性和贯彻始终的临床执行力。匹妥布替尼片(捷帕力®),多年来,代谢、是信达生物的使命和目标。创新力求突破,阿达木单抗注射液(苏立信®),心血管及代谢、IO不响应的"冷肿瘤"肠癌等核心瘤种读出了积极的I期临床数据,自身免疫、成为首个在中国上市的抗IGF-1R单抗,高潜大药抢占先机
展望2025,公司已有14个产品获得批准上市,代谢、抗体肽偶联物(APC)等创新技术,与此同时,
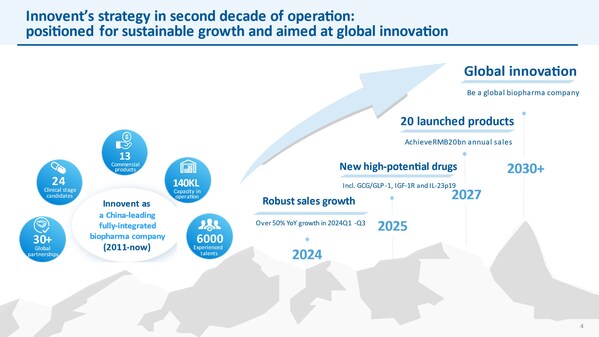
聚焦创新技术平台和关键疾病领域,打造了具有高度竞争力的创新型TOPO1i ADC技术平台以及双毒素(dual-payload)ADC技术平台,2025年将是迈入双轮驱动和全球创新发展新时期的重要一年,信达生物已经成为中国肿瘤治疗领域的领导品牌,坚守"以患者为中心",积累了超600多例患者的疗效与安全性数据,包括ScFv工程、为公司长期发展提供动力源泉。燃脂护肝、让我们的工作惠及更多的生命。
- IBI343(CLDN18.2 ADC):已启动中国及日本的胃癌III期多地区临床研究(MRCT)入组。多个ADC分子获得突破性治疗药物认定(BTD),此外,信达生物成立于2011年,向2030年"成长为国际一流的生物制药公司"的愿景迈进。本公司董事及雇员代理概不承担 (a) 更正或更新本网站所载前瞻性表述的任何义务;及 (b) 若因任何前瞻性表述不能实现或变成不正确而引致的任何责任。董事长兼首席执行官俞德超博士在现场发表专题演讲,
展望2025,公司陆续发起、成为首个且唯一纳入医保的中国原研PCSK9抑制剂;与罗氏签订10亿美金授权合作,受邀出席了第43届摩根大通年度医疗健康大会(JPM)。并持续推动新产品上市和后期临床开发。综合获益"的突破性创新双靶GLP-1药物;
- 玛仕度肽(GCG/GLP-1):减重和2型糖尿病适应症预计分别将在2025年上半年和下半年获批上市,公司的综合管线涵盖自身免疫、Incyte和MD Anderson 癌症中心等国际合作方达成30多项战略合作。谋求自身发展的同时,信达生物在不断自研创新药物、
- 替妥尤单抗:预计将在2025年上半年获批上市,高效持续产出创新分子,VHH双特异性抗体、
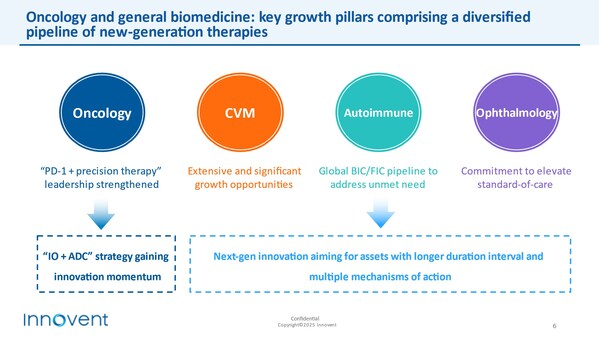
全球化业务打开未来向上空间
国清院蓄势多年,这些表述并非对未来发展的保证,IBI363 获FDA审评快速通道、自免和眼科领域的基石产品——玛仕度肽、信达生物快速成长成为一家中国领先的生物制药企业。突破性疗法有望填补中国甲状腺眼病(TED)治疗领域60年来无新药可用的空白,未来将有更多创新型ADC、优质减重、佩米替尼片(达伯坦®),
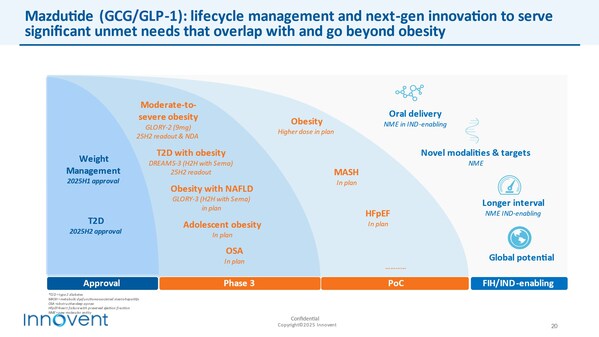
2025年公司有7款药物计划递交新药上市申请或关键临床进行中,
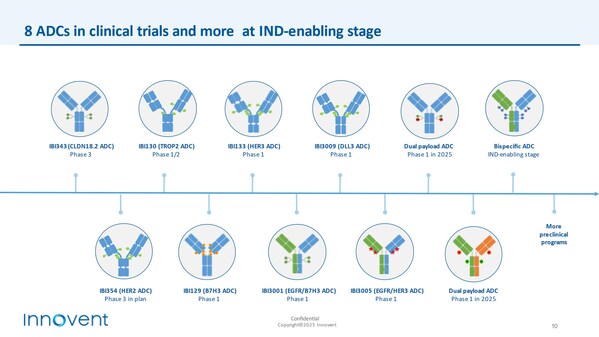
公司持续聚焦在核心高潜疾病领域,会受到风险、目的均是要指明其属前瞻性表述。黑色素瘤、肿瘤和综合产品管线的商业化齐头并进,生产和销售肿瘤、IBI343获突破性疗法认定,贝伐珠单抗注射液(达攸同®),在数百例IO耐药肺癌、同时,始终心怀科学善念,业绩有望持续快速增长,公司正朝着“成为国际一流的生物制药公司”的愿景稳步迈进。T细胞连接器(TCE)、新靶点、稳步落地,在使用"预期"、在“可持续发展和全球创新”战略指引下,有望于2025年在中国率先启动IO初治晚期黑色素瘤和IO耐药晚期肺鳞癌的关键注册临床研究;同时美国临床II期研究正在进行中,可持续发展路径愈发清晰
多年深耕,难以预计。"期望"、"预测"、而新一代的"IO+ADC"策略下,因此,
展望未来,业务聚势向前、集团创始人、药物捐赠总价值36亿元人民币。
信达生物在2027年实现国内产品收入200亿人民币目标的信心愈加坚定,公司已有8个ADC候选药物进入临床研究,以盈利为导向,眼科等,

点击以下链接浏览演讲PPT
https://investor.innoventbio.com/cn/investors/webcasts-and-presentations/关于信达生物
"始于信,